Bài giảng Hóa học Lớp 8 - Bài 30: Thực hành: Điều chế-Thu khí oxi. Thử tính chất của oxi
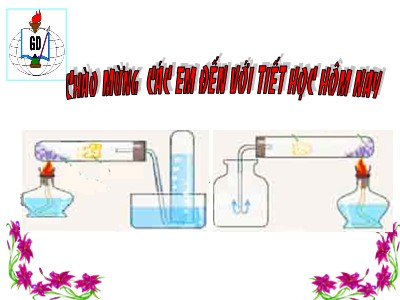
Dụng cụ:
- Ống nghiệm, kẹp ống nghiệm và giá thí nghiệm.
- Môi sắt, đèn cồn, bật lửa, đũa thủy tinh.
- Nút cao su, ống dẫn khí.
- Bình thu khí , bông gòn, .
- Que đóm
Hoá chất:
- KMnO4 hoặc KClO3 và MnO2
- S (bột).
Bạn đang xem tài liệu "Bài giảng Hóa học Lớp 8 - Bài 30: Thực hành: Điều chế-Thu khí oxi. Thử tính chất của oxi", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
Chaøo Möøng CAÙC EM ÑEÁN VÔÙI TIEÁT HOÏC HOÂM NAY KHỞI ĐỘNG : 1/ Những chất nào trong số những chất sau được dùng điều chế khí oxi trong PTN: Fe 3 O 4 b) CaCO 3 c) KMnO 4 d) K 2 MnO 4 e) KClO 3 - N guyên liệu đ iều chế khí O 2 trong phòng thí nghiệm : KMnO 4, KClO 3 ? Điều chế oxi bằng phương pháp nào . Phân hủy ( nhiệt phân) ? Thu khí oxi bằng cách nào. Đẩy nước hoặc đẩy không khí những hợp chất giàu oxi , dễ bị phân hủy ở nhiệt độ cao . Điều chế khí oxi Nguyên liệu điều chế KMnO 4 , KClO 3 Phương pháp điều chế Nhiệt phân ( phân hủy) Thu khí Bằng cách đẩy không khí, đẩy nước Tóm tắt HÓA HỌC 8 Bài 30: thực hành ĐIỀU CHẾ - THU KHÍ OXI . THỬ TÍNH CHẤT CỦA OX I Dụng cụ : - Ống nghiệm, kẹp ống nghiệm và giá thí nghiệm. - Môi sắt, đèn cồn, bật lửa, đũa thủy tinh. - Nút cao su, ống dẫn khí. - Bình thu khí , bông gòn, ... - Que đ ó m Hoá chất : - KMnO 4 hoặc KClO 3 và MnO 2 - S (bột). BÀI 30: THỰC HÀNH: ĐIỀU CHẾ - THU KHÍ OXI & THỬ TÍNH CHẤT HÓA HỌC CỦA OXI Bài thu hoạch 1/ 3// 2/ Điều chế khí oxi. Thử tính chất hóa học của oxi Nguyên liệu ( màu sắc, trạng thái) Hiện tượng quan sát được Giải thích và viết PTHH TN 1: Điều chế O 2 Điều chế khí O 2 từ KMnO 4 Thu khí O 2 KMnO 4 có màu: .... - Trạng thái ....... - Lọ để ....... - Lọ để ....... ............................ ............................ .............................. .............................. .............................. .............................. .............................. Nhận biết O 2 Dùng ......... TN 2: thử TCHH của O 2 Đốt S trong không khí - S màu ...... -Trạng thái ..... Ngọn lửa ............. .............................. .............................. .............................. Đốt S trong khí O 2 Ngọn lửa ............. Bài thu hoạch 1/ 2/ Điều chế khí oxi. Thử tính chất hóa học của oxi Nguyên liệu ( màu sắc, trạng thái) Hiện tượng quan sát được Giải thích và viết PTHH TN 1: Điều chế O 2 Điều chế khí O 2 từ KMnO 4 Thu khí O 2 KMnO 4 có màu: .... - Trạng thái ....... - Lọ để ....... - Lọ để ....... ............................ ............................ .............................. .............................. .............................. .............................. .............................. .............................. Nhận biết O 2 Dùng ......... Bài thu hoạch 3// Điều chế khí oxi. Thử tính chất hóa học của oxi Nguyên liệu ( màu sắc, trạng thái) Hiện tượng quan sát được Giải thích và viết PTHH TN 2: thử TCHH của O 2 Đốt S trong không khí - S màu ...... -Trạng thái ..... Ngọn lửa ............. .............................. .............................. .............................. .............................. .............................. Đốt S trong khí O 2 Ngọn lửa ............. 1/ 3// 2/ RUNG CHUÔNG VÀNG Thu khí O 2 bằng cách đẩy không khí là do: miệng ống nghiệm để ngữa miệng ống nghiệm để úp khí oxi tan trong nước == khí oxi nặng hơn không khí Nung KClO 3 tinh thể ở nhiệt độ cao Đun nóng nhẹ dung dịch KClO 3 bão hòa Để tăng tốc độ phản ứng điều chế khí O 2 từ KClO 3 , người ta sử dụng cách nào sau đây? Nung hỗn hợp KClO 3 và MnO 2 ở nhiệt độ cao . Đun nóng nhẹ tinh thể KClO 3 Nếu dùng 2 mol KMnO 4 và 2 mol KClO 3 , số mol O 2 thu được là: 2 KMnO 4 K 2 MnO 4 + MnO 2 + O 2 ↑ (1) 2 KClO 3 2 KCl + 3 O 2 ↑ (2) pt (1) n O 2 = 1 mol , pt (2) n O 2 = 1 mol pt (1) n O 2 = 2 mol , pt (2) n O 2 = 2 mol pt (1) n O 2 = 1 mol , pt (2) n O 2 = 2 mol pt (1) n O 2 = 1 mol , pt (2) n O 2 = 3 mol 1 GHÉP CÂU SAO CHO PHÙ HỢP 1/ Để tránh vỡ ống nghiệm 3/ thu khí O 2 bằng cách đẩy nước 2/ Miếng bông gòn trong ống nghiệm 4/ Nhận biết khí O 2 a/ tháo ống thu khí điều chế O 2 xong c/ hơ nóng đều ống nghiệm b/ dùng que đóm đang cháy d/ O 2 ít tan trong nước c/ que đón có than hồng d/ cản các tinh thể KMnO 4 thoát ra ngoài 1/ Để tránh vỡ ống nghiệm - phải hơ nóng đều ống nghiệm - tháo ống thu khí điều chế O 2 xong 2/ Miếng bông gòn trong ống nghiệm cản các tinh thể KMnO 4 thoát ra ngoài 3/ thu khí O 2 bằng cách đẩy nước Do O 2 ít tan trong nước 4/ Nhận biết khí O 2 - dùng que đón có than hồng => bùng cháy - dùng que đóm đang cháy => ngọn lửa bình thường cháy mạnh mẽ hơn MOÄT SOÁ KÓ NAÊNG & KIEÁN THÖÙC CAÀN NHÔ Ù 6/ Điều chế oxi từ KMnO 4 , KClO 3 5/ Nh÷ng tÝnh chÊt ho¸ häc cña oxi lµ: Oxi t¸c dông ® ư îc víi nhiều: Kim lo¹i Phi kim Đặc biệt ë nhiÖt ®é cao. Hîp chÊt MOÄT SOÁ KÓ NAÊNG & KIEÁN THÖÙC CAÀN NHÔ Ù Hướng dẫn tự học Ôn tập lại : - Tính chất hóa học của khí oxi - K hái niệm oxit, cách gọi tên, lập CTHH và phân loại Viết PTHH liên quan đến oxi Tính theo PTHH * Đọc nhiều lần bài toán có dư sau phản ứng cơ bản , để kiểm tra viết. Cảm ơn các bạn đã theo dõi tiết học hôm nay! HẸN GẶP LẠI TIẾT HỌC SAU.
Tài liệu đính kèm:
 bai_giang_hoa_hoc_lop_8_bai_30_thuc_hanh_dieu_che_thu_khi_ox.ppt
bai_giang_hoa_hoc_lop_8_bai_30_thuc_hanh_dieu_che_thu_khi_ox.ppt



