Bài giảng Hóa học Lớp 8 - Tiết 45: Luyện tập
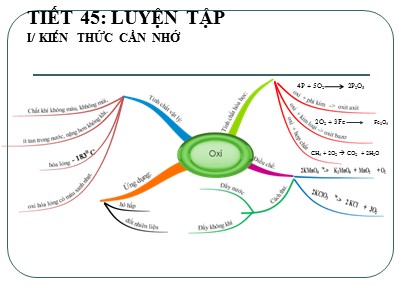
Sự tác dụng của oxi với 1 chất gọi là sự oxi hóa
Oxit là hợp chất của hai nguyên tố, trong đó có một nguyên tố là oxi . Oxit có thể phân chia oxit thành hai loại chính :
Oxit axit Oxit bazơ
Không khí là hỗn hợp nhiều chất khí. Thành phần theo thể tích của không khí là : 78% khí nitơ, 21% khí oxi, 1% các khí khác ( Khí cacbonic, hơi nước, khí hiếm )
Phản ứng hóa hợp là phản ứng hóa học trong đó chỉ có 1 chất mới ( sản phẩm) được tạo thành từ hai hay nhiều chất ban đầu.
Phản ứng phân huỷ là phản ứng hoá học trong đó một chất sinh ra hai hay nhiều chất mới
Bạn đang xem tài liệu "Bài giảng Hóa học Lớp 8 - Tiết 45: Luyện tập", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
TIẾT 45: LUYỆN TẬP I/ KIẾN THỨC CẦN NHỚ 4P + 5O 2 2P 2 O 5 2O 2 + 3Fe Fe 3 O 4 CH 4 + 2O 2 CO 2 + 2H 2 O - Sự tác dụng của oxi với 1 chất gọi là sự oxi hóa - Phản ứng hóa hợp là phản ứng hóa học trong đó chỉ có 1 chất mới ( sản phẩm) được tạo thành từ hai hay nhiều chất ban đầu. - Oxit là hợp chất của hai nguyên tố, trong đó có một nguyên tố là oxi . Oxit có thể phân chia oxit thành hai loại chính : Oxit axit Oxit bazơ - Phản ứng phân huỷ là phản ứng hoá học trong đó một chất sinh ra hai hay nhiều chất mới - Không khí là hỗn hợp nhiều chất khí. Thành phần theo thể tích của không khí là : 78% khí nitơ, 21% khí oxi, 1% các khí khác ( Khí cacbonic, hơi nước, khí hiếm ) I/ KIẾN THỨC CẦN NHỚ sgk II. Bài tập. ( Chú ý chép bài tập và làm vào vở nhé) Bài tập 1. Viết PTHH biểu diễn sự cháy trong oxi của các đơn chất: Cacbon, Photpho, Hiđro, nhôm , biết rằng sản phẩm là những hợp chất có công thức hoá học: CO 2 , P 2 O 5 , H 2 O, Al 2 O 3 . Đáp án . 1) C + O 2 CO 2 . 2) 4P + 5O 2 2P 2 O 5 3) 2 H 2 + O 2 2H 2 O 4) 4Al + 3O 2 2Al 2 O 3 . t 0 t 0 t 0 t 0 Bài tập 2; Hoàn thành các PTHH sau và xác định phản ứng hóa hợp , phản ứng phân hủy a) HgO t0 ---> ? + O 2 b) Cu + O 2 t0 ---> ? c)KClO 3 t0 ---> ? + ? d) ? + ? t0 - --> P 2 O 5 §¸p ¸n: a) 2HgO t0 -> 2Hg + O 2 b) 2Cu + O 2 t0 -> 2CuO c) 2KClO 3 t0 2KCl + 3O 2 d) 4P + 5O 2 t0 2P 2 O 5 ph¶n øng ph©n hñy : a , c ph¶n ønghãa hîp: b, d t 0 t 0 t 0 t 0 t 0 Bài tập 3. Phương trình hóa học trong đó xảy ra sự oxi hóa : 2 KCl + 3O 2 2. 2KMnO 4 K 2 MnO 4 + O 2 + MnO 2 3. O 2 + C CO 2 4. 5O 2 + 4P 2P 2 O 5 5. 2O 2 + 3Fe Fe 3 O 4 1. 2KClO 3 Bài tập 4 : Cho các oxit sau , hãy chỉ ra đâu là oxit axit , đâu là oxit bazơ? Vì sao? K 2 O, Ag 2 O, N 2 O 5 , SO 2, CuO, CO 2 , P 2 O 5, MgO, SiO 2 , FeO. Gọi tên các oxit đó. *Oxit axit *Oxit bazơ N 2 O 5 :đinitơ pentaoxit K 2 O :Kali oxit SO 2 : Lưu huỳnh đioxit Ag 2 O : Bạc oxit CO 2 : Cacsbon đioxit CuO : đồng (II) oxit P 2 O 5 : điphotpho pentaoxit MgO :Magiê oxit SiO 2 :Silic đioxit FeO: Sắt (II) oxit vì là oxit của phi kim và tương ứng với một axit vì là oxit của kim loại và tương ứng với một bazơ ĐÁP ÁN : t 0 Hướng dẫn: a) 2KMnO 4 K 2 MnO 4 + MnO 2 + O 2 b/ - Tìm số mol KMnO 4 n = m/ M =15,8/ 158= 0,1mol 2KMnO 4 K 2 MnO 4 + MnO 2 + O 2 Theo pt 2mol 1mol 1mol 1mol Theo đề 0,1mol ------------- ?mol Có số mol O 2 => V O2(dktc) = n x 22,4 ĐS 1,12lit Bài 5. Trong phòng TN, người ta đun nóng hết 15,8g Kali pemanganat (KMnO 4 ) để thu khí Oxi. a. Viết PTHH? b. Tính thể tích khí Oxi thu được ở đktc? t 0 Bài tập 8 ( phần a/101 SGK) : Để chuẩn bị cho buổi thí nghiệm thực hành của lớp cần thu 20 lọ khí oxi , mỗi lọ có dung tích 100ml . Tính khối lượng kali pemanganat (KMnO 4 ) phải dùng, giả sử khí oxi thu được ở điều kiện tiêu chuẩn và hao hụt 10% : Bài tập 8 ( phần a/101 SGK) : Để chuẩn bị cho buổi thí nghiệm thực hành của lớp cần thu 20 lọ khí oxi , mỗi lọ có dung tích 100ml . Tính khối lượng kali pemanganat (KMnO 4 ) phải dùng, giả sử khí oxi thu được ở điều kiện tiêu chuẩn và hao hụt 10% - Thể tích khí oxi cần dùng: - Do hiệu suất phản ứng đạt 90% : Các em ôn tập chương oxi để vào làm bài 15phut : Mà lượng oxi hao hụt 10% nên hiệu suất phản ứng (H) = 100% - 10% = 90%. Áp dụng công thức tính hiệu suất phản ứng theo chất tham gia phản ứng có
Tài liệu đính kèm:
 bai_giang_hoa_hoc_lop_8_tiet_45_luyen_tap.ppt
bai_giang_hoa_hoc_lop_8_tiet_45_luyen_tap.ppt



