Đề kiểm tra học kì I môn Hóa học Lớp 8 - Năm học 2020-2021 - Trường Trung học Cơ sở Liên Xã (Có đáp án)
Phần 1: Câu hỏi trắc nghiệm (4 điểm) Khoanh vào chữ cái đặt trước câu trả lời đúng nhất (0,25đ)
Câu 1. Cho các chất sau đâu là đơn chất, hợp chất, phân tử: O2, H2, P2O5, O3, CH4, CH3COOH, Ca, Cl2. Số chất là đơn chất là
A. 3 B. 4 C. 5 D. 6
Câu 2. Một hỗn hợp gồm bột sắt và bột lưu huỳnh. Có thể dùng dụng cụ nào sau đây để tách riêng bột sắt với bột lưu huỳnh
A. Đũa thủy tinh B. Ống nghiệm C. Nam châm D. Phễu
Câu 3. Hợp chất Alx(SO3)3 có phân tử khối là 342 đvC. Giá trị của x là
A. 1 B. 2 C. 3 D. 4
Câu 4. Cho hợp chất của X là XO và Y là Na2Y. Công thức của XY là
A. XY B. X2Y C. X3Y D. Tất cả đáp án.
Câu 5. Dấu hiệu của phản ứng hóa học
A. Thay đổi màu sắc B. Tạo chất bay hơi C. Tạo chất kết tủa D. Tất cả đáp án
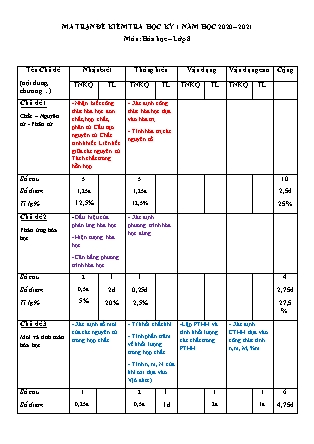
MA TRẬN ĐỀ KIỂM TRA HỌC KỲ 1 NĂM HỌC 2020 – 2021 Môn: Hóa học – Lớp 8 Tên Chủ đề (nội dung, chương ) Nhận biết Thông hiểu Vận dụng Vận dụng cao Cộng TNKQ TL TNKQ TL TNKQ TL TNKQ TL Chủ đề 1 Chất – Nguyên tử - Phân tử - Nhận biết công thức hóa học đơn chất, hợp chất, phân tử. Cấu tạo nguyên tử. Chất tinh khiết. Liên kết giữa các nguyên tử. Tách chất trong hỗn hợp. - Xác định công thức hóa học dựa vào hóa trị. - Tính hóa trị các nguyên tố. Số câu Số điểm Tỉ lệ % 5 1,25đ 12,5% 5 1,25đ 12,5% 10 2,5đ 25% Chủ đề 2 Phản ứng hóa học - Dấu hiệu của phản ứng hóa học. - Hiện tượng hóa học. - Cân bằng phương trình hóa học. - Xác định phương trình hóa học đúng. Số câu Số điểm Tỉ lệ % 2 0,5đ 5% 1 2đ 20% 1 0,25đ 2,5% 4 2,75đ 27,5% Chủ đề 3 Mol và tính toán hóa học - Xác định số mol của các nguyên tử trong hợp chất. - Tỉ khối chất khí. - Tính phần trăm về khối lượng trong hợp chất. - Tính n, m, N của khí oxi dựa vào V(ở đktc) -Lập PTHH và tính khối lượng các chất trong PTHH - Xác định CTHH dựa vào công thức tính n,m, M, %m... Số câu Số điểm Tỉ lệ % 1 0,25đ 2,5% 2 0,5đ 5% 1 1đ 10% 1 2đ 20% 1 1đ 10% 6 4,75đ 47,5% Tổng số câu 8 1 8 1 1 1 20 Tổng số điểm 2 2 2 1 2 1 10đ Tỉ lệ % 40% 30% 20% 10% 100% (Kèm theo Công văn số 1749/SGDĐT-GDTrH ngày 13/10/2020 của Sở GDĐT Quảng Nam) TRƯỜNG PTDTBT THCS LIÊN XÃ LA ÊÊ – CHƠ CHUN ĐỀ KIỂM TRA HỌC KÌ I NĂM HỌC: 2020 - 2021 Họ và tên HS: MÔN: HÓA HỌC 8 SBD: Phòng thi: ....... Thời gian: 45 phút (không kể thời gian giao đề) Lớp: Điểm Lời phê của giáo viên Chữ ký GT Bằng số Bằng chữ Giám thị 1 Giám thị 2 Phần 1: Câu hỏi trắc nghiệm (4 điểm) Khoanh vào chữ cái đặt trước câu trả lời đúng nhất (0,25đ) Câu 1. Cho các chất sau đâu là đơn chất, hợp chất, phân tử: O2, H2, P2O5, O3, CH4, CH3COOH, Ca, Cl2. Số chất là đơn chất là A. 3 B. 4 C. 5 D. 6 Câu 2. Một hỗn hợp gồm bột sắt và bột lưu huỳnh. Có thể dùng dụng cụ nào sau đây để tách riêng bột sắt với bột lưu huỳnh A. Đũa thủy tinh B. Ống nghiệm C. Nam châm D. Phễu Câu 3. Hợp chất Alx(SO3)3 có phân tử khối là 342 đvC. Giá trị của x là A. 1 B. 2 C. 3 D. 4 Câu 4. Cho hợp chất của X là XO và Y là Na2Y. Công thức của XY là A. XY B. X2Y C. X3Y D. Tất cả đáp án. Câu 5. Dấu hiệu của phản ứng hóa học A. Thay đổi màu sắc B. Tạo chất bay hơi C. Tạo chất kết tủa D. Tất cả đáp án Câu 6. Phương trình đúng là A. P + O2 → P2O3 B. Na + H2SO4 → Na2SO4 + H2 C. Zn + 2HCl → H2 + ZnCl2 D. Mg + O2 → MgO Câu 7. Hiện tượng nào sau đây không phải là hiện tượng hóa học? A. Đốt cháy đường B. Thở hơi thở làm đục nước vôi trong. C. Đốt cháy cồn D. Mực hòa tan vào nước Câu 8. Trong các khí sau, số khí nhẹ hơn không khí là: CO2, H2O, N2, H2, SO2 A. 5 B. 4 C. 3 D. 2 Câu 9. Nguyên tử có khả năng liên kết với nhau nhờ A. Electron B. Proton C. Nơtron D. Tất cả đều đúng Câu 10. Tính % mK có trong phân tử K2CO3 A. 56, 502% B. 56,52% C. 56,3% D. 56,56% Câu 11. Chất nào sau đây được coi là tinh khiết A. Nước cất B. Nước suối C. Nước khoáng D. Nước đá từ nhà máy Câu 12. Một oxit có công thức là Fe2O3. Hóa trị của Fe trong oxit là A. I B. II C. III D. IV Câu 13. Trong nguyên tử hạt nào mang điện tích âm A. electron B. Notron C. Proton D. proton và notron Câu 14. Ta có một oxit tên CrO. Vậy hợp chất của Crom có hóa trị tương ứng là A. CrSO4 B. Cr(OH)3 C. Cr2O3 D. Cr2(OH)3 Câu 15: Công thức hóa học của axit nitric (biết trong phân tử có 1H, 1N, 3O) là: A. HNO3 B. H3NO C. H2NO3 D. HN3O Câu 16 : Trong các công thức hóa học sau, công thức hóa học nào sai A. K2O B. BaNO3 C. ZnO D. CuCl2 Phần 2. Tự luận (6 điểm) Câu 1. (2 điểm) Chọn hệ số thích hợp để cân bằng các phản ứng sau: a) MgCl2 + KOH → Mg(OH)2 + KCl b) Cu(OH)2 + HCl → CuCl2 + H2O c) Fe2O3 + 2H2SO4 → Fe2(SO4)3 + 2H2O d) NO2 + O2 + H2O → HNO3 Câu 2. (1 điểm) Hãy cho biết 33,6 lít khí oxi (đktc) a) Có bao nhiêu mol oxi? b) Có bao nhiêu phân tử khí oxi? c) Có khối lượng bao nhiêu gam? d) Cần phải lấy bao nhiêu gam khí N2 để có số phân tử gấp 4 lần số phân tử có trong 3.2 g khí oxi. Câu 3. (2 điểm) Đốt cháy hoàn toàn 13 gam Zn trong oxi thu được ZnO. a) Lập phương trình hóa học. b) Tính khối lượng ZnO thu được? c) Tính khối lượng oxi đã dùng? Câu 4. (1 điểm) Một hợp chất khí có thành phần % theo khối lượng là 82,35% N và 17,65% H. Xác định công thức hóa học của chất đó. Biết tỉ khối của hợp chất khí với hidro bằng 8,5. (H = 1; O = 16, Fe = 56, S = 32, Na = 23, Mg = 24, Al = 27, N = 14, C = 12, Ca = 40) ----------HẾT---------- BÀI LÀM Phần 1. Trắc nghiệm khách quan mỗi câu đúng 0,25 điểm Câu 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 Đáp án Phần 2. Tự luận . Đáp án Đề thi học kì 1 hóa 8 năm học 2020 - 2021 Phần 1. Trắc nghiệm khách quan mỗi câu đúng 0,25 điểm Câu 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 Đáp án C C B A D C D D A B A C A A A B Phần 2. Tự luận Câu Nội dung Điểm 1 a) MgCl2 + 2KOH → Mg(OH)2 + 2KCl b) Cu(OH)2 + 2HCl → CuCl2 + 2H2O c) Fe2O3 + 2H2SO4 → Fe2(SO4)3 + 2H2O d) 4NO2 + O2 + 2H2O → 4HNO3 0,5 0,5 0,5 0,5 2 a) nO2 = 33,6/1,5 = 3 mol b) Số phân tử oxi bằng: 1,5.6,023.1023 = 9,0345.1023 phân tử c) mO2 = nO2.MO2 = 1,5.32 = 48 gam d) Số mol oxi có trong 1,6 gam: nO2 = 1,6/32 = 0,05 mol => nN2 = 3.0,05 = 0,15 mol => mN2 = 0,15.28 = 4,2 gam 0,25 0,25 0,25 0,25 3 a) PTHH: 2Zn + O2 → 2ZnO b) Số mol Zn là: nZn = 13/65 = 0,2mol PTHH: 2Zn + O2 → 2ZnO Tỉ lệ PT: 2mol 1mol 2mol 0,2mol ? mol ? mol Số mol ZnO tạo thành là: nZnO = (0,2.2)/2= 0,2mol => Khối lượng ZnO là: mZnO = 0,2 . 81 = 16,2 gam c) Số mol khí O2 đã dùng là: nO2= (0,2.1)/2 = 0,1mol => Khối lượng O2 là: mO2 = n.M = 0,1.32 = 3,2gam 0,5 0,25 0,25 0,25 0,25 0,25 0,25 4 Khối lượng mol của hợp chất khí bằng: M = d,MH2 = 8.5,2 = 17 (gam/mol) Số mol nguyên tử của mỗi nguyên tố trong 1 mol hợp chất: Trong 1 phân tử hợp chất khí trên có: 1mol nguyên tử N và 3 mol nguyên tử H. Công thức hóa học của hợp chất trên là NH3 0,25 0,25 0,25 0,25 Giáo viên bộ môn Coor Viếu Tổ trưởng chuyên môn
Tài liệu đính kèm:
 de_kiem_tra_hoc_ki_i_mon_hoa_hoc_lop_8_truong_trung_hoc_co_s.docx
de_kiem_tra_hoc_ki_i_mon_hoa_hoc_lop_8_truong_trung_hoc_co_s.docx



